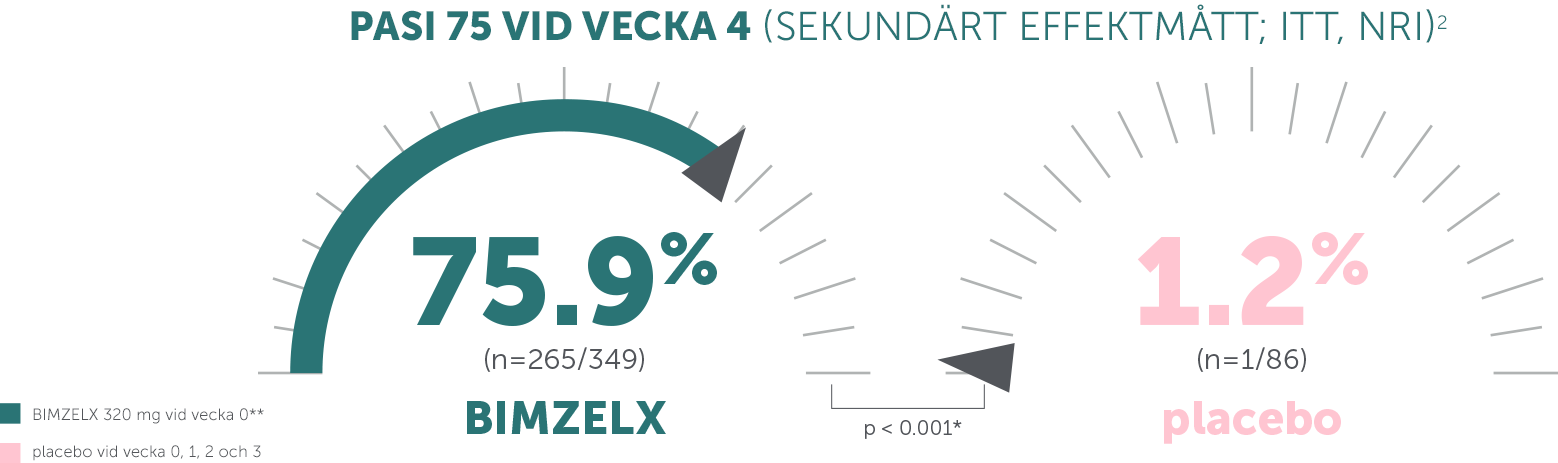
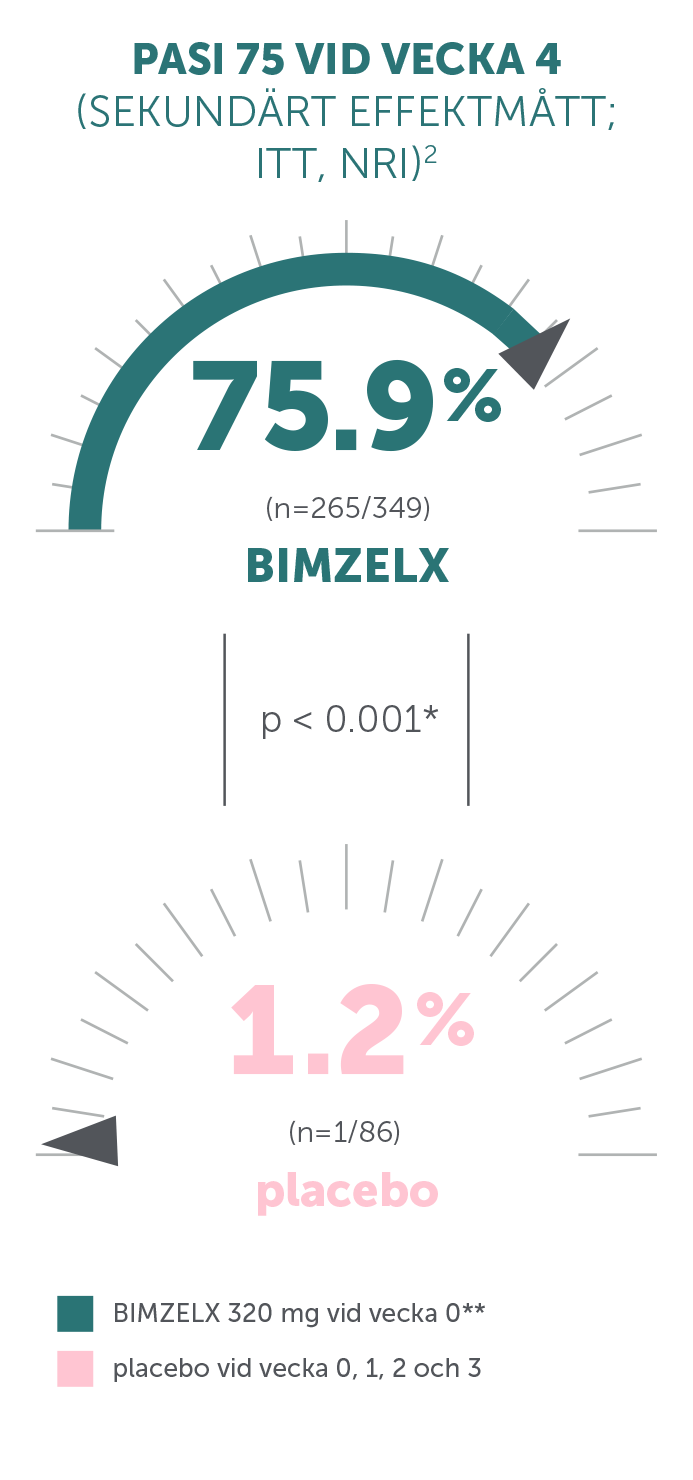
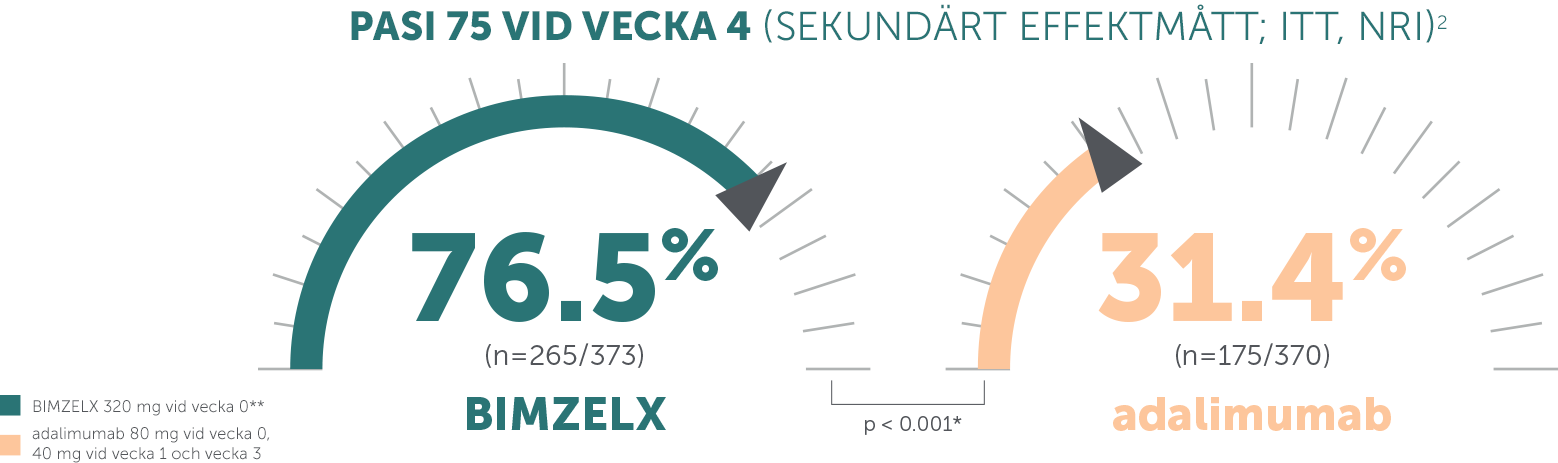
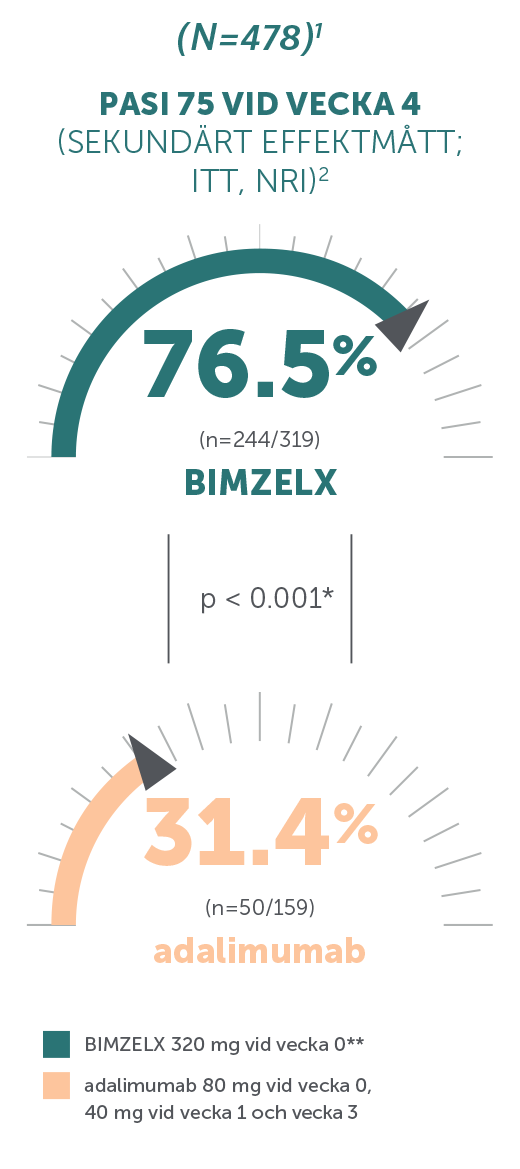
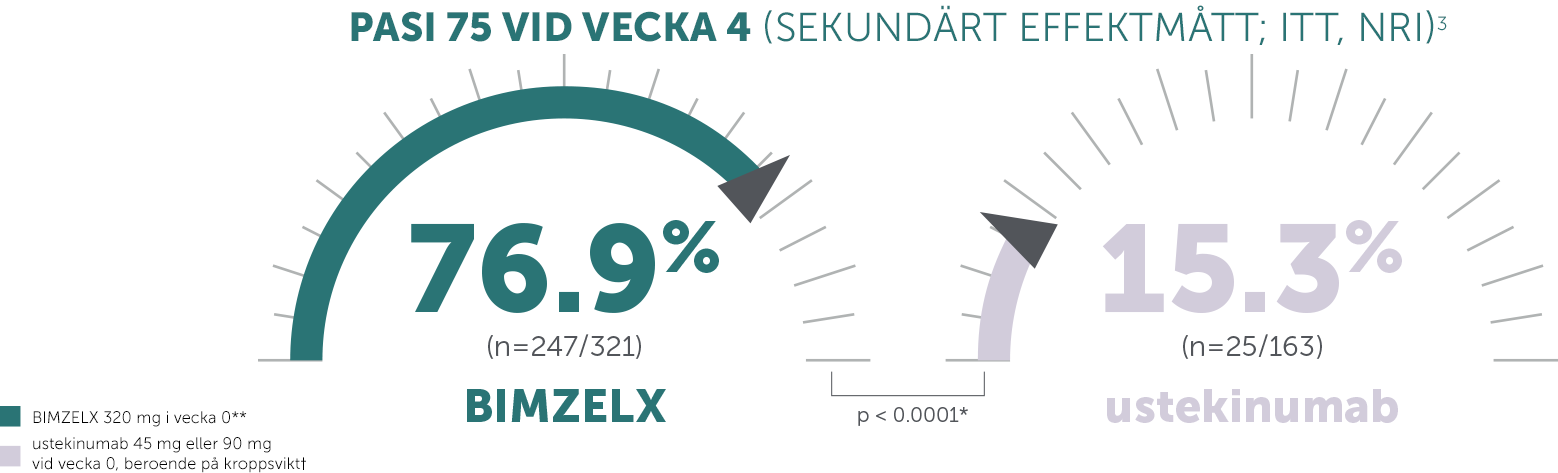
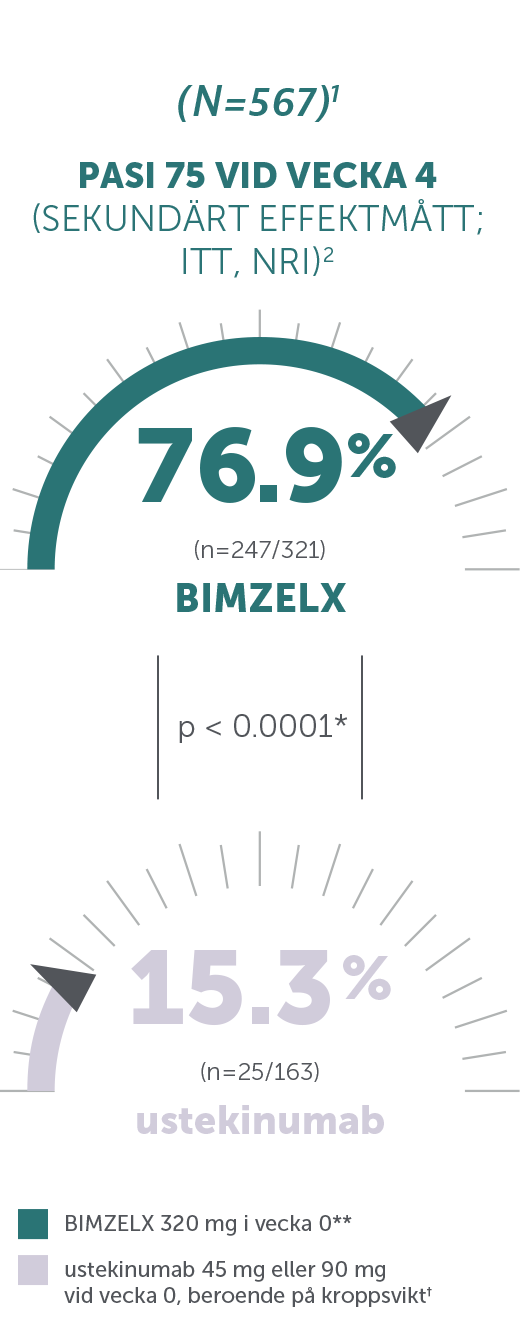
BIMZELX: snabbt insättande effekt (vecka 4 efter första dosen) jämfört med ustekinumab och adalimumab1–3
PRIMÄRA EFFEKTMÅTT: i BE SURE (N = 478) hade 86,2 % uppnått PASI 90 vid vecka 16 med BIMZELX jämfört med 47,2 % med adalimumab (samprimärt effektmått, p < 0,001);2 i BE VIVID (N = 567) hade 85,0 % uppnått PASI 90 vid vecka 16 med BIMZELX jämfört med 4,8 % med placebo (p < 0,0001)3,4

SE-P-BK-PSO-2100039 Datum för utarbetande: okt 2021
BIMZELX är indicerat för behandling av måttlig till svår plackpsoriasis hos vuxna personer som behöver systemisk behandling.1
Få åtkomst till BIMZELX förskrivningsinformation via navigeringsfältet längst upp på varje sida.
Förkortad förskrivningsinformation Bimzelx® (bimekizumab).
Beredningsform: 160 mg lösning i förfylld spruta och förfylld injektionspenna. Varje förfylld spruta eller förfylld penna innehåller 160 mg bimekizumab i 1 mL Rx, (F), L04AC21.
Indikation: Bimzelx® är indicerat för behandling av: 1. Måttlig till svår plackpsoriasis hos vuxna som behöver systemisk behandling, 2. Aktiv ankyloserande spondylit (AS) hos vuxna med tidigare otillräcklig respons på eller intolerans mot konventionell behandling, 3. Aktiv icke-radiografisk axial spondylartrit (nr-axSpA) med objektiva tecken på inflammation påvisat genom förhöjt C-reaktivt protein och/eller magnetkameraundersökning hos vuxna med tidigare otillräcklig respons på eller intolerans mot icke-steroida antiinflammatoriska läkemedel (NSAID) samt 4. Aktiv psoriasisartrit hos vuxna med tidigare otillräckligt svar eller intolerans mot ett eller flera sjukdomsmodifierande antireumatiska läkemedel (DMARDs) där bimekizumab kan ges i monoterapi eller i kombination med metotrexat.
Dosering och administreringssätt: Den rekommenderade dosen för vuxna patienter med plackpsoriasis är 320 mg (som ges som 2 subkutana injektioner på 160 mg vardera) vid vecka 0, 4, 8, 12, 16 och därefter var 8:e vecka. Den rekommenderade dosen för patienter med AS, nr-axSpA och psoriasisartrit är 160 mg (ges som 1 subkutan injektion på 160 mg) var 4:e vecka. För patienter med psoriasisartrit och samtidig måttlig till svår plackpsoriasis är den rekommenderade dosen densamma som för plackpsoriasis och baserat på kliniskt svar i lederna kan efter vecka 16 behandling med 160 mg var 4:e vecka övervägas. Ingen dosjustering krävs för patienter över 65 års ålder. Bimekizumab har inte studerats i patientpopulationer med nedsatt njur- eller leverfunktion. Säkerhet och effekt för bimekizumab hos barn och ungdomar yngre än 18 år har inte fastställts.
Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne. Kliniskt betydelsefull aktiv infektion (t.ex. aktiv tuberkulos (TB)).
Varning och försiktighet: Bimekizumab kan öka risken för infektioner såsom övre luftvägsinfektioner och oral kandidos. Försiktighet bör iakttas då man överväger att använda bimekizumab till patienter med kronisk infektion eller anamnes på återkommande infektion. Bimekizumab ska inte ges till patienter med aktiv TB. Patienter som får bimekizumab bör övervakas avseende tecken och symtom på aktiv TB. Behandling mot TB bör övervägas innan behandling med bimekizumab påbörjas hos patienter med anamnes på latent eller aktiv TB för vilka en adekvat behandlingskur inte kan bekräftas. Bimekizumab rekommenderas inte till patienter med inflammatorisk tarmsjukdom. Allvarliga överkänslighetsreaktioner inklusive anafylaktiska reaktioner har observerats med IL-17-hämmare. Överväg att slutföra alla lämpliga vaccinationer enligt aktuella riktlinjer för åldersgruppen innan behandling med bimekizumab påbörjas. Levande vacciner ska inte ges till patienter som behandlas med bimekizumab. Fertila kvinnor ska använda en effektiv preventivmetod under pågående behandling och i minst 17 veckor efter avslutad behandling.
Biverkningar: mycket vanliga (≥ 1/10): övre luftvägsinfektioner; vanliga (≥ 1/100, < 1/10): oral kandidos, tineainfektioner, öroninfektioner, herpes simplex-infektion, orofaryngeal kandidos, gastroenterit, follikulit, huvudvärk, dermatit och eksem, akne, reaktioner på injektionsstället, trötthet; mindre vanliga (≥ 1/1 000, < 1/100): mukös och kutan kandidos (inklusive esofageal kandidos), konjunktivit, neutropeni, inflammatorisk tarmsjukdom.
Läkemedelsförmån: Subventioneras endast för behandling av plackpsoriasis och psoriasisartrit för patienter som inte har fått tillräcklig effekt av TNF-hämmare eller där detta inte är lämpligt.
Datum för översyn av produktresumén: Sept 2023. För fullständig produktinformation och pris se www.fass.se. UCB Pharma AB, Olof Palmes gata 29, 111 22 Stockholm. Tel 040-294900.
▼ Detta läkemedel är föremål för utökad övervakning. Detta möjliggör snabb identifiering av ny säkerhetsinformation. Vårdgivare uppmanas att rapportera misstänkta biverkningar.
BSA, Body Surface Area; Cl, konfidensintervall; CMH, Cochran-Mantel-Haenszel; IGA, Investigator's Global Assessment; ITT, intention to treat; NRI, non-responder imputation; OLE, öppen förlängningsfas; PASI 75/90/100, ≥75/≥90/100 % förbattring från baslinjen för psoriasissjukdomens utbredning och svårighetsgrad; Q1W, varje vecka; Q4W, var fjärde vecka; Q8W, var åttonde vecka; Q12W, var tolfte vecka.
*Saknade data tillskrevs non-responder imputation; p-värden för jämförelse av behandlingsgrupper baserades på CMH-testet från den allmänna associationen.1-3
**Den rekommenderade dosen för vuxna patienter med plackpsoriasis är 320 mg (ges som 2 subkutana injektioner om 160 mg vardera) vid vecka 0, 4, 8, 12, 16 och var åttonde vecka därefter. Man bör överväga att avbryta behandlingen hos patienter som inte uppvisat någon förbättring efter 16 veckors behandling. För vissa patienter med en kroppsvikt på ≥ 120 kg som inte uppnått fullständig läkning av huden vid vecka 16 kan 320 mg var fjärde vecka efter vecka 16 förbättra behandlingssvaret ytterligare.1
‡Ustekinumabdosen baserades på patientens kroppsvikt vid baslinjen (45 mg for patienter som vägde ≤ 100 kg eller 90 mg för patienter som vägde ≥ 100 kg) och var oförändrad under resten av prövningen.3
Referenser
- BIMZELX SmPC 2021, available from: https://www.ema.europa.eu/en/documents/product-information/bimzelx-epar-product-information_sv.pdf
- Warren RB, Blauvelt A, Bagel J, et al. Bimekizumab versus adalimumab in moderate to severe plaque psoriasis. N Engl J Med. 2021;385(2):130-141.
- Reich K, Papp KA, Blauvelt A, et al. Bimekizumab versus ustekinumab for the treatment of moderate to severe plaque psoriasis (BE VIVID): efficacy and safety from a 52-week, multicentre, double-blind, active comparator and placebo controlled phase 3 trial. Lancet. 2021;397(10273):487-498.
- Reich K, Papp KA, Blauvelt A, et al. Bimekizumab versus ustekinumab for the treatment of moderate to severe plaque psoriasis (BE VIVID): efficacy and safety from a 52-week, multicentre, double-blind, active comparator and placebo controlled phase 3 trial. Lancet. 2021;397(10273):487-498. Supplementary appendix.