
Certolizumab pegol
Vad är Certolizumab Pegol?
En annan molekylär struktur
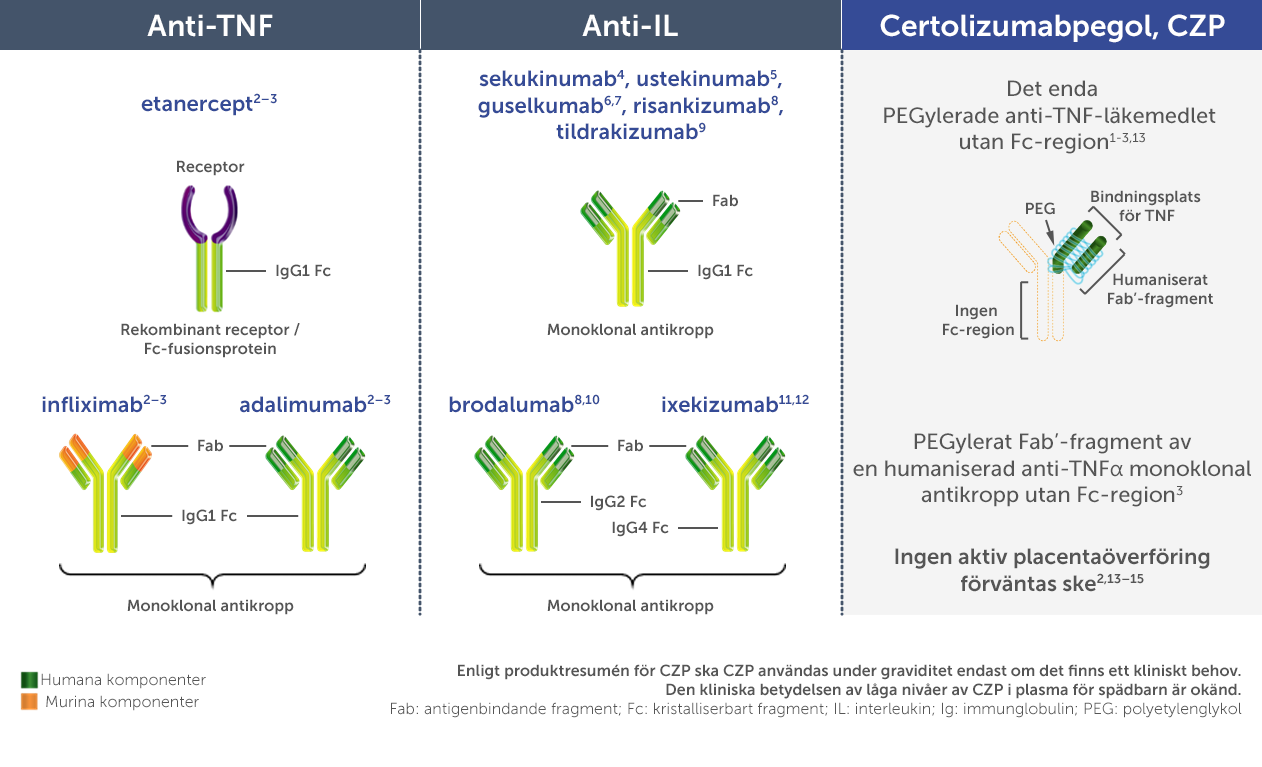
Certolizumab Pegol (CZP) är ett humaniserat Fab’-fragment mot tumörnekrosfaktor alfa (TNFα) och är konjugerat till polyetylenglykol (PEG)1. Denna konjugering till PEG gör det möjligt för CZP att förlänga den terminala halveringstiden för eliminering i plasma till ca 14 dagar1. För patienter med måttlig till svår plackpsoriasis är CZP det enda Fc-fria biologiska medlet som finns tillgängligt. Tack vare denna Fc-fria struktur förväntas inte CZP genomgå aktiv placentaöverföring.1,2,13–15
Tillgänglig för patienter sedan 2009
Certolizumab Pegol (CZP) godkändes av Europeiska läkemedelsmyndigheten 2009 för behandling av måttlig till svår aktiv reumatoid artrit. Sedan dess har CZP också godkänts och indikerats för svår aktiv axial spondylartrit, bestående av ankyloserande spondylit och icke-radiografisk axial spondylartrit, aktiv psoriasisartrit och måttlig till svår plackpsoriasis hos vuxna patienter.1

Psoriasis
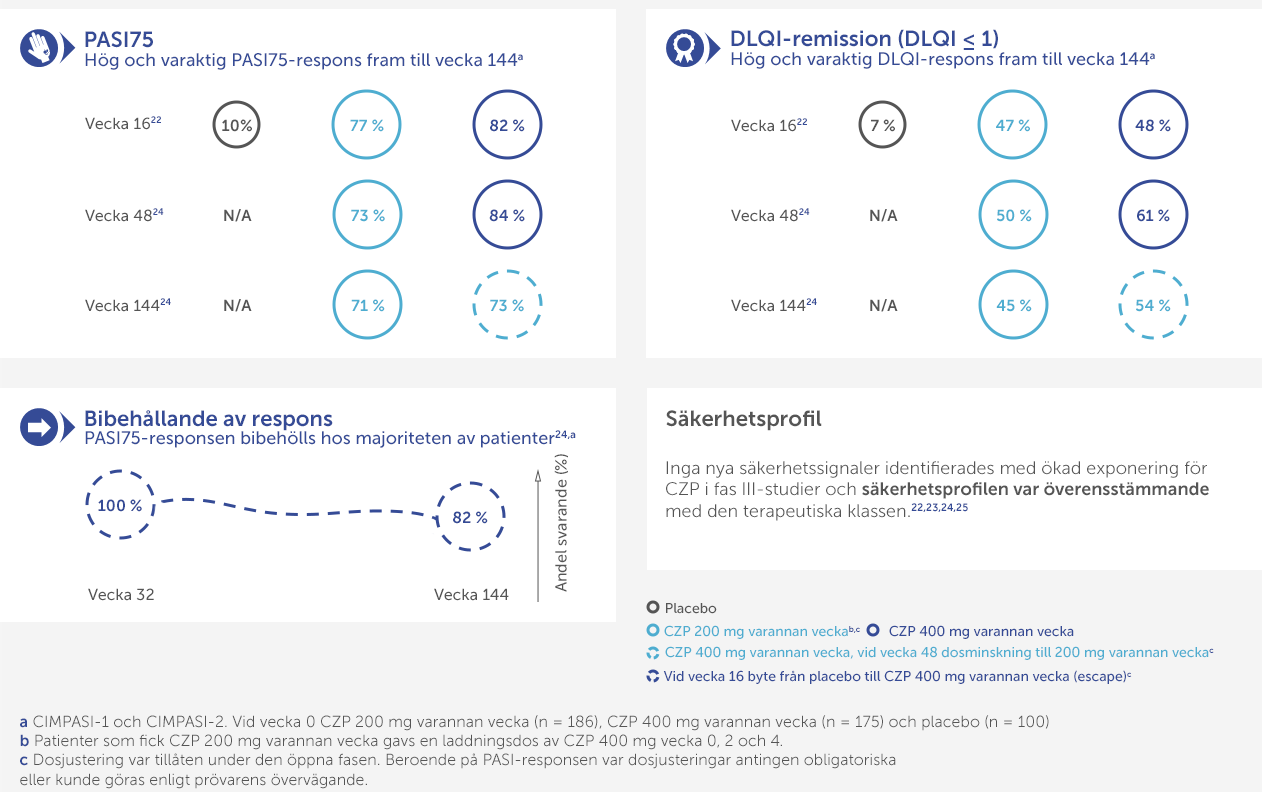
Doseringen av Certolizumab Pegol (CZP) består av en initial laddningsdos (400 mg vecka 0, 2 och 4), och sedan en underhållsdos för vuxna patienter med plackpsoriasis som är 200 mg varannan vecka. För underhållsbehandling kan en dos på 400 mg varannan vecka övervägas för patienter med otillräckligt svar.1
Effekt och säkerhet för CZP har visats hos 1 112 patienter med måttlig till svår plackpsoriasis i kontrollerade och öppna fas III-studier i upp till 3 år: CIMPASI 1, CIMPASI 2 och CIMPACT.1, 22-25
Psoriasisartrit
Psoriasis förknippas med flera viktiga medicinska tillstånd28, inklusive psoriasisartrit. Därför är det viktigt att visa att Certolizumab Pegol också har visat effekt och säkerhet på kort sikt (jämfört med placebo) och på lång sikt (upp till 4 år).
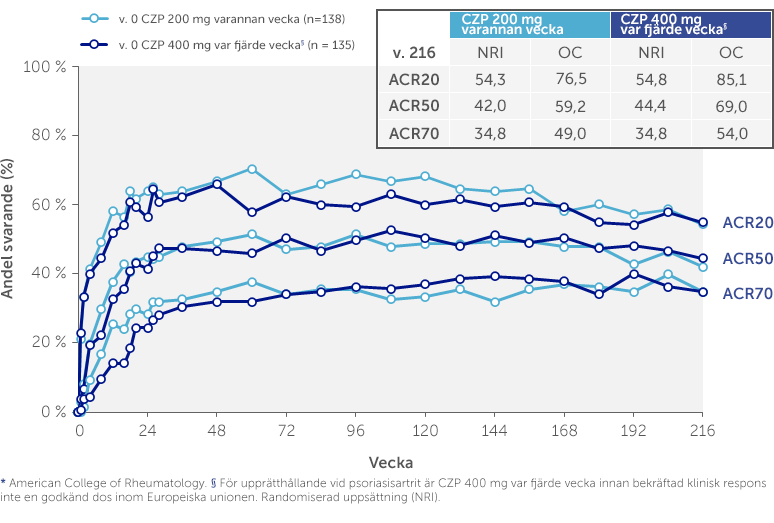
Bibehållen effekt av ACR*-svar från vecka 24 till vecka 216
Kvinnor i fertil ålder
Vi fortsätter att bidra till forskningen och förbättringar av vården av kvinnor som lever med svåra kroniska sjukdomar under deras fertila ålder. UCB har genomfört 2 farmakokinetiska studier och har har kontinuerligt analyserat resultaten av graviditeter i vår farmakovigilans-databas för att kunna ge aktuell och tydligt information till sjukvårdspersonal och patienter.
Data från graviditeter ger möjlighet till fortsatt behandling av kvinnor i fertil ålder när kliniskt behov föreligger30
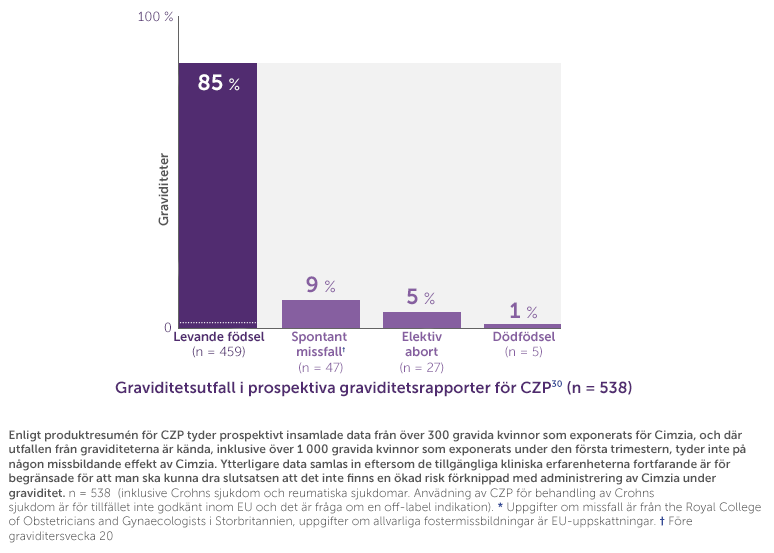
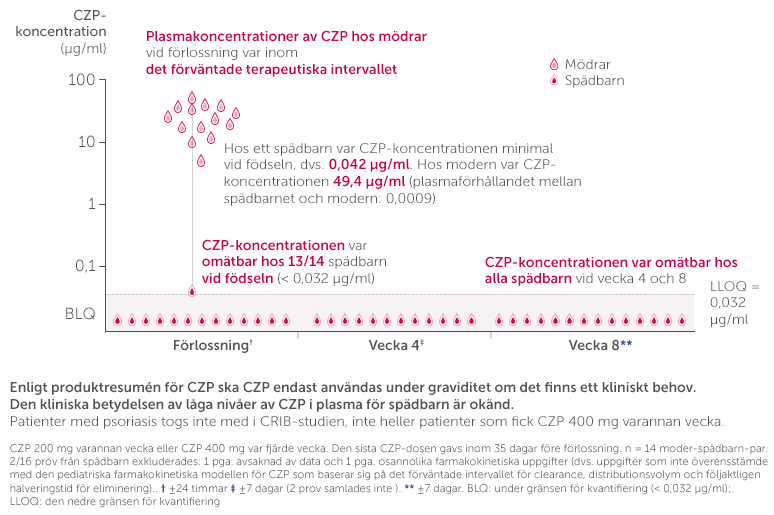
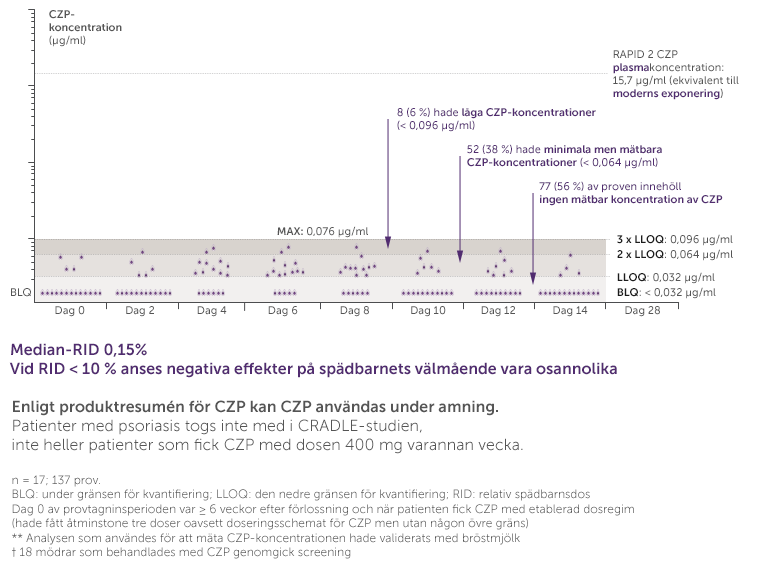
Certolizumab Pegol visade ingen till minimal (<0,1 %) placentaöverföring från moder till foster15
Referenser
- CIMZIA® Produktresumé. Finns på https://www.ema.europa.eu/en/documents/product-information/cimzia-epar-product-information_en.pdf. Hämtad maj 2022.
- Hyrich KL et al. Rheumatology (Oxford). 2014;53:1377–1385.
- Weir N et al. Therapy. 2006;3:535–545.
- Secukinumab - EPAR Public Assessment Report EMA/CHMP/489954/2014. Finns på https://www.ema.europa.eu/en/documents/product-information/cosentyx-epar-product-information_en.pdf. Hämtad maj 2022.
- Benson JM et al. mAbs. 2011;3(6):535–545.
- Jeon C et al. Human Vaccines & Immunotherapeutics. 2017;13(10):2247–2259.
- EMA. Guselkumab (Tremfya®) Produktresumé. 2019. p2. https://www.ema.europa.eu/en/medicines/human/EPAR/tremfya
- Kaplon H and Reichert JM. mABs. 2018;f10(2):183–203.
- EMA. Tildrakizumab (Ilumetri®) Produktresumé. 2019. p2, 6. https://www.ema.europa.eu/en/medicines/human/EPAR/ilumetri
- EMA. Brodalumab (Kyntheum®) Produktresumé. 2019. p2, 7. https://www.ema.europa.eu/en/medicines/human/EPAR/kyntheum
- Liu L et al. J Inflamm Res. 2016;9:39–50.
- EMA. Ixekizumab (Taltz®) Produktresumé. 2019. p2, 8. https://www.ema.europa.eu/en/medicines/human/EPAR/taltz#product-information-section
- Wakefield I et al. Toxicol Sci. 2011;122:170–176.
- Porter C et al. J Reprod Immunol. 2016;116:7–12.
- Mariette X et al. Ann Rheum Dis. 2018;77:228–233.
- EPAR (RA). Finns på https://www.ema.europa.eu/en/documents/assessment-report/cimzia-epar-public-assessment-report_en.pdf. Hämtad maj 2022.
- Certolizumab pegol Produktresumé. Finns på http://www.ema.europa.eu/docs/en_GB/document_library/EPAR__Product_Information/human/001037/WC500069763.pdf. Hämtad maj 2022.
- CHMP summary of opinion (axSpA). Finns på https://www.ema.europa.eu/en/documents/smop/chmp-post-authorisation-summary-positive-opinion-cimzia_en-0.pdf. Hämtad maj 2022.
- CHMP summary of opinion (PsA). Finns på https://www.ema.europa.eu/en/documents/smop/chmp-post-authorisation-summary-positive-opinion-cimzia_en-1.pdf. Hämtad maj 2022.
- CHMP summary of opinion (PSO). Finns på https://www.ema.europa.eu/en/documents/smop/chmp-post-authorisation-summary-positive-opinion-cimzia-ii-65_en.pdf. Hämtad maj 2022.
- Curtis JR et al. RMD Open. 2019;5:e000942.
- Gottlieb AB et al. J Am Acad Dermatol. 2018;79(2):302−314.e6.
- Lebwohl M et al. J Am Acad Dermatol. 2018;79(2):266−276.e5.
- Gordon K et al. Br J Dermatol. 2021;184:652–662.
- Blauvelt A et al. JEADV. 2019;33:546–552.
- Blauvelt A et al. Br J Dermatol. 2020. doi:10.1111/bjd.19314.
- Warren RB et al. JEADV. 2021;35(12):2398–2408.
- Griffiths CEM et al. Lancet. 2021;397:1301–1315.
- van der Heijde D, Deodhar A, Fitzgerald O, Fleischmann R, Gladman D, Gottlieb AB et al. 4-Year Results From the Rapid PsA Phase 3 Randomised Placebo-Controlled Trial of Certolizumab Pegol in Psoriatic Arthritis. RMD Open. 2018;4:e000582.
- Clowse MEB et al. Arthritis Rheum. 2018;70(9):1399–1407.
- Clowse MEB et al. Ann Rheum Dis. 2017;76:1890–1896.
Framställningsdatum: maj 2022
SE-P-CZ-PSO-2200003
© UCB Biopharma SRL, 2021. Alla rättigheter förbehållna.